
LA CHAPA DE COBRE EN CUBIERTAS.
Sin lugar a dudas y sin depreciar a ninguno de los otros metales que se pueden emplear en cubiertas, el cobre es inigualable, ofrece una belleza singular propia, acompañada de un durabilidad incomparable. Sus propiedades son de sobra conocidas, dan al material una vida dinámica ofreciendo cambios impresionantes en lo que a su tonalidad se refiere sin alterar en absoluto su resistencia. la cubierta de cobre es inconfusa, se identifica por su color desde el primer día, desde su color natural va tornado a un color oscuro negruzco que varía hacia un azul verdoso característico exclusivo que solo el cobre ofrece. Además, la chapa de cobre, por sus características, permite al artesano instalador trabajarla a su mejor intuición sin riesgo.
Trabajar una cubierta de cobre es como hacer traje a medida, con el mejor paño. Por eso merece de una un oficio bien formado que sea capaz de lograr con su trabajo poesía. La cubierta de cobre tiene que deleitar al mirarla, para eso hay que armonizar las formas, los pliegues, el sentido de las chapas, el esmero en la instalación hasta conseguir el exclusivo traje.
Desde hace muchos años se viene utilizando la chapa de cobre más bien en edificaciones singulares en los que el proyectista busca originalidad y distinción, por eso su instalación exige de esmero para conseguir armonización con el resto de la edificación. La cubierta de cobre siempre va a ir asociada a una construcción de nobleza y superior calidad.
Con todo lo antes dicho encumbrando el material, no cabe duda que hay poco margen para que una cubierta de cobre fracase o se arruine. Sería impensable que una cubierta de cobre termine inservible exigiendo de su retirada, sin embargo sucede que muchas, muchas cubiertas de cobre presentan un deterioro lamentable, ¿ y esto porqué? Si el metal es el más resistente y duradero ¿ cuál puede ser la causa de que haya que retirar o reparar profundamente una cubierta de cobre ? la respuesta es nítida, el oficio o la planificación son los elementos causantes. Claro, también puede haber causas fortuitas, pero son las menos, en cualquier caso, la causa fortuita va permitir siempre una reparación eficaz y nunca exigirá la retirada de la cubierta por inservible.
Hay algo muy controvertido ¿ y sí la cubierta funciona y exige de su retirada ? parece inconcuso, inverosímil , incomprensible que haya que retirar una cubierta de cobre que está funcionando, que la chapa está servible, que permanece su impermeabilidad, pero hay que recogerla .
No olvidemos la definición de la palabra cubierta, que no es otra que cubrir y que la definición no tiene nada que ver con soporte o estructura, sin embargo la cubierta está asociada por necesaria al soporte y el soporte a la estructura de cubierta. Dicho esto, si falla el soporte, falla necesariamente la cubierta y corre riesgo la estructura de cubierta.

Con frecuencia insisto en la importancia del soporte, de la vital importancia que tiene para el buen funcionamiento de la cubierta. En este caso me ciño a hablar de cobre, no de otros materiales sobre los que también en ocasiones me pronuncio y como dato doy el que por ejemplo; el soporte puede alterar la chapa de zinc. Sin embargo, el soporte no va alterar la chapa de cobre, pues ya he mencionado el cobre como un material resistente a la agresividad de ácidos o a la corrosión, es un metal que se puede considerar noble.
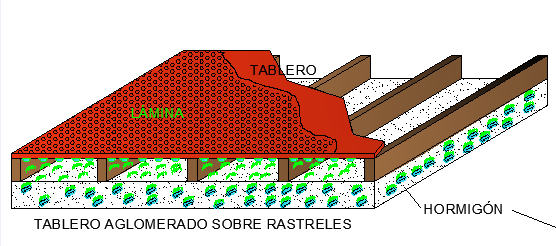
Desafortunadamente se sigue el ritmo de proyectar, de hacer cubiertas de cobre sobre soportes vulnerables que no van acorde con la durabilidad que ofrece el cobre. Se siguen proyectando e instalando cubiertas de cobre sobre tableros prefabricados mediando una lámina entre el tablero y la chapa. Se siguen instalando cubiertas de cobre sobre tableros tipo Sándwich terminados en tablero hidrófugo y lámina intermedia y nadie se pronuncia del sin sentido del sistema.

Ya de por sí, el hecho de trabajar con un material de tan alta calidad y pensar en simple tablero de apoyo, dotarlo de una lámina intermedia, invita a reflexionar sobre la ignorancia de quien lo prescribe o consiente. Solo hace falta que medie la lógica o el sentido común para entender que eso es una tropelía, no digamos si se tienen unos conocimientos básicos de física. o si de vez en cuando se destinase un poquito de tiempo a pensar.
Si nos queremos documentar, solo hace falta ver alguna cubierta de cobre antigua y sobre lo que se asienta la chapa, desde luego que sobre tablero no va a estar instalada, entre otras cosas porque no los había en la época que se hizo la cubrición, pero si había madera maciza y sobre eso está la chapa de cobre. Por el contrario y para documentarnos también; muchas cubiertas de cobre de nueva época, realizadas con los avances y conocimientos más recientes están inservibles. ¿qué es lo que falla? Parece que el cobre que es el que tiene que impermeabilizar es el que ofrece más dudas, o sino para que se ponen láminas protectoras bajo la chapa con ese razonamiento irónico de que si el cobre falla, siempre queda la lámina, es decir, que se da más importancia a una simple lámina que al metal noble. Claro, lo que nadie se pregunta es ¿ y qué papel terminara desempeñando la lámina soportando el calórico que le transmite el cobre y que pasará con el vapor o aire húmedo que se almacene entre la lámina y el tablero? ahí está la clave, en el vapor o aire húmedo que pulule entre la lámina y el tablero, sencillamente será que la humedad va a terminar pudriendo, así como suena pudriendo el tablero, descomponiéndolo volviéndolo en nomenclatura a su inicio, es decir a serrín.

¿Son eficientes los tableros Sándwich o los tableros prefabricados para soportar directamente una cubierta de cobre o? rotundamente no por las condiciones físicas que se dan entre la chapa y el soporte Y ¿qué pasa cuando el tablero se pudre? Sencillamente el cobre queda libre de fijaciones y la cubierta saldrá desplazada. es decir, que el cobre sigue funcionando pero el soporte desaparecido y no solo eso, que a la vez que se va pudriendo el soporte entran en oxidación los elementos de fijación estructurales.
Queda así explicado como una cubierta de máxima calidad puede resultar desastrosa a consecuencia del soporte.
Todo lo dicho en este artículo no es antojo del autor, no, responde a muchas realidades que sumadas me invitaron a articular este artículo que está amparado por veracidad pasada y reciente.
Recientemente hemos retirado una cubierta de cobre que parecía intacta, no daba ningún problema de humedad, sin embargo estaba próxima a desplazarse . Hubo que planificar minuciosamente un sistema que paso por retirar la chapa de cobre, los restos de tablero, fijación de la capa de tablero interior y aislamiento a la estructura, instalación de un nuevo soporte a base de entablado de madera de pino sobre rastreles ,sin más, sobre la tabla directamente chapa de cobre.
Manuel Álvarez












 Las mansardas están cubiertas con chapas romboidales individuales (tipo teja) gozan de un meticuloso ensamblaje que las hace definitivamente impermeables, todas ellas van fijadas individualmente al entablado de la forma más peculiar ( impensable en nuestro tiempo ) . Nada menos que 11 buhardas sobresalen de las cuatro mansardas. Estas buhardillas están totalmente cubiertas de zinc ornamentado, son de una singular belleza, dan a entender que han sido realizadas a propósito para esta empresa, pues las hemos llegado a ver similares en troquelados pero no en fabricación artesanal. Igualmente destacan las cumbreras y otros apliques que sí son de serie, tal vez llegados de algún taller Belga a juzgar por otros similares que hemos encontrado. Como de
Las mansardas están cubiertas con chapas romboidales individuales (tipo teja) gozan de un meticuloso ensamblaje que las hace definitivamente impermeables, todas ellas van fijadas individualmente al entablado de la forma más peculiar ( impensable en nuestro tiempo ) . Nada menos que 11 buhardas sobresalen de las cuatro mansardas. Estas buhardillas están totalmente cubiertas de zinc ornamentado, son de una singular belleza, dan a entender que han sido realizadas a propósito para esta empresa, pues las hemos llegado a ver similares en troquelados pero no en fabricación artesanal. Igualmente destacan las cumbreras y otros apliques que sí son de serie, tal vez llegados de algún taller Belga a juzgar por otros similares que hemos encontrado. Como de 















Debe estar conectado para enviar un comentario.