
CUBIERTAS DE CHAPA DE ZINC
El zinc, se utiliza en construcción como material de cobertura desde hace muchísimos años, si bien en las últimas décadas su empleo ha sido masivo al menos en nuestro país.
Antaño, se empleaba la chapa de zinc para la cubrición de edificios muy singulares y ornamentaciones destacadas, curiosamente se observa más en ciudades portuarias, quizá por las facilidades del transporte y la importación de otras culturas.
La instalación, antiguamente era muy artesanal, las ornamentaciones eran de serie, estampados idénticos que se repetían en la mayoría de los ornamentos incluso fuera de nuestras fronteras. Diferentes culturas arquitectónicas han utilizado mucho el zinc en sus edificios emblemáticos, tanto para cubrirlos como para adornarlos con majestuosas cúpulas y chapiteles. Podemos contemplar algunas edificaciones muy antiguas cubiertas con chapas de zinc romboidales o de pico, que en la actualidad están intactas, lo que viene a significar que el zinc es metal fiable.
En España, a diferencia de otros países con más cultura en la instalación, el trabajo de colocar el zinc se reservaba a los ojalateros, por aquello de que sabían estañar y contaban en sus talleres con algunas herramientas con las que podían manufacturar las chapas, generalmente alguna plegadora. El empleo principal era en canalones, bajantes y escasas cubiertas de chapiteles, miradores, fachadas o algún que otro palco ornamentado en plazas públicas.
En otros países, si podemos ver edificios muy antiguos cubiertos totalmente con zinc.
Curiosamente, en España, hasta hace unos años hemos contado con una importante fabrica de zinc, concretamente en Lugones, la que se llamo Asturiana de zinc, allí, se laminaba y se servía en chapas de 200×100 cm. y se sellaban con los nº 10,12 y 14,
El bum de construcción que hemos vivido, trajo consigo el empleo masivo de materiales que apenas antes se empleaban. El Zinc, sin lugar a dudas, se adapta a cualquier tipo de construcción y no deja de aportar cierta identidad asociada con la calidad. A la vez que se promocionaba el empleo de zinc en cubiertas, empezaron a aparecer máquinas, herramientas, diferentes ofertas de acabados y accesorios, que los mismos vendedores facilitaban a los espontáneos instaladores. La falta de oficio y escasa cultura en el conocimiento del comportamiento del metal, no tardo en dejarse notar con resultados muy negativos incluso la ruina de muchas cubiertas.
A la hora de planificar una cubierta de chapa de zinc, es conveniente tener en cuenta algunos factores, por ejemplo: la ubicación de la edificación, su complejidad y muy importante el soporte, entendiendo este último como elemento con el que la chapa va a estar en contacto permanente. Igualmente es importante el definir bien los diversos remates y el modo de resolverlos. Partiremos de la base de que la chapa de zinc tiene muy poco grosor, tiene un coeficiente de dilatación muy alto, La dilatabilidad del zinc cambia a diferentes temperaturas.
Es de potencial negativo (-0,76) con respecto al hidrógeno, por tanto tendente a ceder electrones, por otra parte su coeficiente de dilatación es muy alto.
Se debe de atender especialmente a procurar que las chapas gocen de libertad para moverse y su soporte sea compatible. A diferencia de lo que se suele recomendar como una cámara de ventilación efectiva, si tenemos en cuenta algunos resultados, la cámara de ventilación es de dudosa necesidad. Volvemos a insistir que es más importante que el soporte no ofrezca dudas. También se debe huir de hacer chapas demasiado largas, más recomendable es hacerlas cortas, no más allá de los 5 metros cuidándose de que las fijaciones garanticen la movilidad. Por supuesto, los encuentros y remates, si no se pueden garantizar con pliegues, hay que utilizar estaño al 50%, jamás se deben resolver con masillas o siliconas. A ser posible la estructura ha de tener suficiente pendiente para que al menos no haya posibilidad de que quede agua estancada, pues en las zonas de estancamiento se suelen acumular residuos sólidos, estos pueden portar ácidos, a la vez que terminan siendo altamente higroscópicos y pueden provocar corrosiones en la chapa. En cubiertas que por necesidad tengan poca pendiente,se debe procurar alguna limpieza, máxime si hay vegetación arbórea cercana.
La chapa de zinc, en la actualidad, se sirve mayormente en bobinas de diferentes tonelajes, también de diferentes grosores y acabados. Con esto tenemos suficiente para proyectar el tipo de cubierta de que se nos antoje. Importante tener en cuenta que los diferentes acabados son solo superficiales de la chapa que en teoría se van a ir degradando en el tiempo, si bien ofrecen a priori una perspectiva diferente. Si tomamos como base la chapa de zinc de acabado natural, nos referimos a metal de color plateado muy brillante, que se va a ir transformando, en su parte vista, a consecuencia de la combinación con el aire húmedo de la atmósfera renovada, va a ir creando una capa de carbonato básico e hidróxido, lo que tradicionalmente se llama pátina, ella va a proteger la chapa, su color termina en un gris opaco, entendiéndolo como oscuro y sombrío.
Si tenemos en cuenta que la reacción del zinc a la intemperie es inevitable y a la vez necesaria, pues el recubrimiento de la capa de carbonato va a ser homogénea protegiendo toda la superficie y así a evitar las posibles agresiones atmosféricas u otras. Es de entender que la degradación de las capas de acabado no van a ser homogéneas, por tanto nos sería fácil deducir que en aquellos puntos en los que vaya quedando el zinc limpio, se van a producir la típica reacción soltando a la vez hidróxido, pero el punto que reacciona no se va a ver favorecido por otras aportaciones lo que significa que se va a ir perdiendo materia sin compensación y ello podría provocar alguna picadura, aunque esto no esté científicamente comprobado, si vemos que los pre-patinados son más proclives a reacciones dudosas.
El SOPORTE
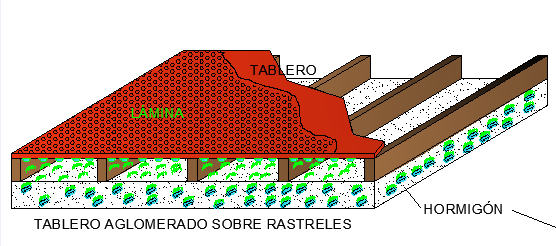
El soporte tiene una importancia vital para la ulterior vida del zinc, se vienen manteniendo una serie de teorías respecto al comportamiento interior de la chapa de zinc y se da como solución más fiable la de procurar una mal llamada cámara de ventilación, se suele aconsejar una lámina alveolar, con su propio nombre comercial. Por el simple hecho de dotar la parte interior de esta lamina parece ser que queda todo resuelto, pero la realidad es, en muchos casos, bien distinta, pues vamos encontrando cubiertas con corrosiones importantes y en su mayoría están dotadas de este sistema de lámina intermedia. Nuestra opinión es que estas láminas sirven únicamente para separar la chapa del soporte que generalmente suele ser tablero aglomerado. Pues es bien sabido que los tableros portan un PH muy alto en acidez y ello termina repercutiendo en la chapa si hay algún tipo de comunicación acuosa, pues ella terminará haciendo de electrolito y se formara una pila entre el tablero y la chapa, cediendo electrones el zinc y quedando con carga positiva, a la postre corrosión garantizada.
Nuestras recomendación es procurar un soporte a base de tablas de madera de pino, sabido es, por estar así demostrado, que la madera de pino esta con un PH entre 5 y 7, por ello es perfectamente compatible y se puede poner el zinc directamente sobre ella, si conviene que la tabla este un poco separada para favorecer el paso de corrientes de aire. Se está observando que aunque se produzcan condensaciones no afectan negativamente al zinc. Sin duda que el soporte de tabla puede resultar un poco más costoso que el tablero, pero el resultado justifica con creces la diferencia de precio que pueda haber. La formula más recomendable es instalar rastreles de madera en el mimo sentido de las pendientes, estos rastreles de 40 x 30 mm. fijados al soporte estructural, bien sea hormigón, o incluso tableros tipo sándwich, llevarán una separación entre 35 y 50 cm. Posteriormente y en sentido perpendicular se realizará el entablado con tablas de no más de 15 cm. de ancho por 22 mm. de grueso, clavadas convenientemente de tal forma que las cabezas de las puntas queden incrustadas y separadas las tablas entre si no más de 20 mm. De esta forma quedara garantida una cámara de aire. Se debe de tener en cuenta, que el zinc no debe de estar en contacto con otros metales, ejemplo el hierro y a ser posible se debe de evitar que reciba aguas procedentes de otros metales, pues ellas pueden transportar iones y repercutir negativamente en la chapa.
LA INSTALACIÓN
Elegiremos un grosor de chapa no exagerado, pero si abundante, se suele comercializar en muchos espesores , podemos citar 0,5, 0,65, 0,7, 0,8, 1 mm. …. 0,7 mm. puede servirnos. De aquí podemos calcular el peso por m/2 que se despejara multiplicando el espesor por la densidad. A ello le añadiremos un porcentaje dependiendo de la complejidad de la cubierta, generalmente se viene aplicando un 25%. Si es junta de listón se puede incrementar un 5%.
La chapa de zinc para cubiertas viene regularizada, puede conducirnos a engaño algunos añadidos tales como “aleado al cobre titanio”. Lo que muchos dan en llamarlo zinc titanio, la realidad es que estos aportes en la fundición son ínfimos y lo vemos más como una cuestión de marketing. Si nos hemos percatado que no todos los fabricantes presentan la chapa con la misma textura de la misma forma que el comportamiento a la hora de irse creando la pátina no es igual en todos. Aunque en términos generales podríamos confiar en que el zinc que está en el mercado es perfectamente apto.
Los sistemas de instalación se mueven entra la junta alzada o la junta de listón. En raras y especiales ocasiones se utiliza también la junta plana. Ofrece cada una de ellas un aspecto muy diferenciado. Tengamos en cuenta que la junta de listón va a presentar un volumen de unos 6 cm. aproximadamente y la junta alzada 2. La junta plana se eleva 1cm. por la anchura que se le quiera dar.


La junta de listón, se llama así por llevar un rastrel de madera de 40 x 40 mm, al que llegarán las chapas a ambos lados plegadas en ángulo recto y posteriormente se cubrirá el rastrel con una capota en forma de U invertida abrazando los pliegues, el rastrel servirá a la vez para soportar las pletinas de fijación que garantizarán el libre movimiento de las chapas. Este tipo de instalación fue el más empleado antaño. Pues era el más cómodo de trabajar con la maquinaria de la época, bastaba con una simple plegadora para hacer toda la manufacturación. Podríamos añadir que la chapa no sufría prácticamente nada en los plegados y quedaba intacta sin resquebrajamientos microscópicos, en definitiva, que podíamos dar como más fiable y duradera la instalación por el sistema de junta de listón.
La junta alzada, es la más extendida, la chapa se manufactura en máquinas especiales que por un sistema de rodillos la van moldeando a ambos lados de tal forma que posteriormente se pueden ir uniendo unas chapas con otras para terminar “engatillandolas” las fijaciones se hacen con grapas que pueden ser fijas o móviles, las móviles permiten el movimiento de las chapas. Este tipo de instalación es mucho más cómoda rápida, a la vez conlleva menos material que la otra citada. Se debe tener especial cuidado a la hora de perfilar, la máquina debe de estar bien ajustada para que la chapa no sufra al irse doblando a la vez también hay que procurar que haya una temperatura más bien elevada , el mismo cuidado, en cuanto a la temperatura habrá que tener cuando se trabaje la instalación y sobre todo cuando nos dispongamos a hacer los engatillados, una temperatura baja puede facilitar la rotura del zinc. El factor temperatura, se debe de tener en cuenta sea cual sea el tipo de instalación. En épocas de invierno, cuando es necesario hacer pliegues, se suele ir calentando previamente la chapa.
La junta plana se suele utilizar para cubriciones muy especificas, de muros, aleros, techos u otras en las que no conlleven mucho o ningún riesgo, pues no son tan seguras como cualquiera de las otras.
Ni que decir tiene que en cualquier tipo de instalación que dispongamos hacer, se debe procurar que las chapas gocen de plena libertad para moverse, no han de estar en contacto con otros elementos metálicos o propios de construcción, se debe de aportar algún separador, ejemplo papel de estraza, e incluso, ante la duda aplicar una mano de minio de plomo. Laminas de zinc, aplicadas directamente sobe ladrillos que contengan al menos 1,4% de sales solubles en tiempo húmedo inmediatamente se corroen, lo que se puede evitar aislando con una capa de fieltro.
Los remates han de resolverse mediante pliegues, engafetados u otros que garanticen la estanqueidad y por supuesto no ofrezcan riesgo de resquebrajarse. Ante la duda se puede acudir al estañado de uniones. Nunca se acudirá a resolver uniones mediante remaches, masillas o siliconas. Cualquier oficial ha de gozar de destreza y habilidad suficiente para resolver los remates debidamente con el propio material, para ello hay herramientas especiales que permiten hacer cualquier tipo de trabajo complicado con las máximas garantías.
LOS CANALONES
Especial importancia tienen los canalones en una cubierta. Creemos que por motivos estéticos, se tiende a proyectar canalones interiores, lo que lleva implícito asumir un importante riesgo, pues cualquier fuga va a repercutir directamente en el interior y se termina sabiendo cuando el agua se hace visible y a traspasado todo el soporte, muchas veces las fugas son ínfimas y cuando se ve la humedad ya ocasionado el gran desastre en el soporte,. Por eso hay que poner especial empeño a la hora A la hora de instalar canalones hay que poner especial empeño d máxime si son interiores o de pesebre como vulgarmente se les suele llamar.
El soporte del canalón ha de ser exactamente igual al que lleve el resto de la cubierta y a poder ser dotarlo de algún elemento aislante, pues se suelen producir fuertes condensaciones. La base, debería de ser semicircular y siempre con pendientes suficientes hacia las bajantes. Las bajantes que han de calcularse con respecto a la superficie de cubierta, entre ellas hay que hacen juntas de dilatación, si puede ser no más lejanas de 6 metros. Por comodidad, se han empleado y aún se emplean juntas de dilatación de neopreno, que consisten en una banda que embebe a ambos lados una chapa de zinc que posteriormente se suelda a las chapas de canalón, esta banda permite los movimientos de las chapas, pero hemos comprobado que no son eficaces, pues terminan rompiéndose, de modo que lo mejor es acudir al sistema tradicional que consiste en: soldar los cabezales de la chapa de canalón, dejarlos separados y cubrirlos con una posterior capota, para esto ha de haber pendiente suficiente para que el agua no se estanque. Pero de poco sirve todo esto si no atendemos a dejar holgura suficiente para que se pueda mover la chapa y a la vez no fijamos debidamente de tal forma que las chapas puedan moverse con absoluta libertad. No es raro ver canalones clavados en vez de estañados, remachados en las uniones y con una capa de silicona.
Las uniones han de estañarse siempre con estaño al 50%.. Solemos recomendar que se hagan unos aliviaderos, que servirán para en caso de obstrucción de las bajantes el agua pueda salir libremente al exterior, pues de lo contrario entraría hacia el interior.
CANALONES COLGADOS
Respecto a los canalones colgados, pueden ser de sección redonda o cuadrada de desarrollo variables, no deberían de exceder de 35 cm. Generalmente son más estables los de sección redonda, pues no acusan tanto las deformaciones y conducen mejor el agua hasta las bajantes.
Se suelen servir en piezas de 2 metros que se irán uniendo con estaño, aunque no es raro verlos unidos con silicona, lo cual nunca se debería hacer. Hay que procurar sus juntas de dilatación, a poder ser no más lejanas de 12 metros, con lo cual entendemos que verterán tramos dos tramos de 6 metros a la misma bajante. Las juntas de deben resolver de la misma forma descrita para los canalones de pesebre. Estos canalones van soportados por unas palomillas que describen la misma figura del canalón y van fijadas al alero, han de ser suficiente rígidas y no quedar demasiado distanciadas, 50 cm. sería lo ideal. Para resolver las esquinas, juntas de dilatación, y bajantes, existen piezas normalizadas que evitan las soldaduras en obra permitiendo así mayor agilidad en la instalación, respecto a las conexiones de bajantes, igualmente existen embocaduras especiales que evitan tener que soldar los tubos directamente contra el canalón a la vez de que permiten una mejor evacuación.
BAJANTES
Las bajantes vienen normalizadas de fábrica, de sección redonda o cuadrada, se sirven en piezas de dos o tres metros , unidas longitudinalmente mediante engatillado o electrosoldadura, son diferentes secciones, las más empleadas son de 80 o 100 mm. han de ir acordes con la sección del canalón que empleemos. Es recomendable en la parte más cercana al canalón poner una cazoleta que a parte de ser un elemento decorativo, sirve mayormente para que en caso de atascamiento el agua se despeje por ella. En la instalación, las bajantes se embocan unas en otras y se fijan fijar a los paramentos verticales mediante abrazaderas. Es conveniente no apretarlas demasiado para que puedan moverse en caso de dilataciones.
REPARACIONES
REPARACIÓN DE CUBIERTAS DE ZINC.
¿Cuál es la causa que obliga a las reparaciones?
En teoría, una cubierta de zinc no tendría que ocasionar ningún problema y por tanto no requerir de reparaciones, pero la realidad es bien distinta. Nadie se supone a priori, que una cubierta de chapa de zinc llegue a tener filtraciones de agua suponiéndola como funcional en el tiempo.
Concebimos el material como un material noble y duradero, que además da un aspecto singular y de carácter a cualquier edificación. Por otra parte, hay una variada oferta de acabados que, se amoldan a las necesidades estéticas más exigentes imaginables por cualquier facultativo de la construcción que quiera dar una nota añadida de singularidad a sus obras. ¿ pero, que está ocurriendo?.
Con el paso del tiempo, vamos asistiendo a ritmos cada vez más agigantados a la vista de cubiertas que están dando serios problemas de agrietamientos y de corrosiones. Ello requiere de un análisis en profundidad para averiguar las principales causas y así poder llegar a remedios eficaces. Lamentablemente muchas veces se llega tarde y la solución conlleva únicamente al desmontaje integral de la cubierta y su soporte.
El zinc, está perfectamente concebido para su utilización como material de cubrición y así lo demuestran infinidad de obras realizadas por todo el mundo. Son conocidas cubiertas muy longevas y sin acusar más problemas que los típicos de cualquier cubierta, quizá que por falta de mantenimiento haya engroses de elementos sólidos sobre la cubierta o en los canalones, algún ínfimo fallo en remates complicados.
Tenemos que diferenciar esos resultados negativos provenientes de causas típicas de otros más preocupantes como pueden ser las corrosiones.
Aún en la actualidad se están resolviendo algunos remates con siliconas o masillas y sabido es que eso no funciona en el tiempo. Los remates han de hacerse con plegados o soldándolos con estaño al 50%, atendiendo siempre a las posibles dilataciones y también a un buen oficio que sepa de soldadura, pues para este tipo de .practicas hay que disponer de un buen oficio desayunado en pericia.
Vemos con frecuencia Canalones unidos con elementos sintéticos al igual que juntas de dilatación resueltas con materiales de caucho o neopreno. Estos, por lo que hemos visto en algunas zonas tienen una vida limitada no más allá de los 6 años, parecido ocurre con las juntas resueltas con sellados. Aunque también nos encontramos con soldaduras de estaño reventadas. En el primer caso, ya sabemos que las soluciones con elementos sintéticos no son las óptimas ni van acordes con la durabilidad de la chapa de zinc. En el segundo caso, cuando el estaño revienta es causa de déficit en la aplicación.
Cuando se acomete una reparación de esos elementos que no funcionan hay que recurrir a tratarlos como si fuese de origen, es decir, eliminar los elementos que no funcionan, sanear las zonas afectada y empezar de nuevo con plegados o estañados cueste lo que cueste, lo que nunca se debería de hacer es parchear sobre lo hecho, pues así lo único que conseguimos es agravar el problema. Pongamos un ejemplo acompañado de imágenes. Si en un canalón no funcionan las juntas selladas, eliminamos los sellados, limpiamos y soldamos debidamente y así tendremos el problema resuelto. No se debe acudir a otros elementos y claro que si se puede estañar, de no poder hacerlo se sustituye la parte afectada y se hace de nuevo. Lo mismo ocurre con los agrietamientos en las chapas. Hartos estamos de ver como se cubren con telas o pinturas, no estamos en desacuerdo con estos materiales, pero sirven para lo que sirven, no para solucionar definitivamente problemas sobre la superficie de la chapa de zinc.
Mención muy distinta meren las corrosiones de la chapa. Este asunto nos trae de cabeza, pues para entendernos, se trata de que la chapa de zinc se va descomponiendo. No vemos que muchos se atrevan a hablar de este fenómeno tan frecuente. Asistimos en diferentes puntos de nuestra geografía a demasiadas cubiertas que acusan este fenómeno y vemos también que nadie se atreve a hablar de él. La corrosión de la chapa de zinc es el principal problema de ruina de muchas cubiertas. Ya lo hemos comentado al principio, la chapa de zinc no debería dar ni el más mínimo problema, eso sí, trabajándola en unas condiciones determinadas.
Cuando ocurre este fenómeno, ya demasiado extendido, nadie se pone de acuerdo en cual es la causa, pero la hay, claro que la hay. Lo llamativo es que la mayoría de las corrosiones, al menos las que nosotros hemos observado, son de interior a exterior. Entendemos que esto no debería de suceder cuando multitud de instaladores han seguido a pies juntos las recomendaciones de vendedores los que auguraban que con una cámara de ventilación estaba todo resuelto. Claro que sí, intermediando una lámina magistral entre tableros y chapa no habría problemas, pero el resultado es exageradamente distinto y eso se ve. ¿Cual es pues la causa? Y por otro lado ¿cabe solución a estos problemas?
Nota: Texto e imágenes están protegidas por derechos de autor, no se autoriza el copiado ni la divulgación por ningún medio sin el permiso por escrito del propio autor.
Manuel Álvarez.





























Debe estar conectado para enviar un comentario.